Circles reshape the RNA world(点击左边标题下载原文)
Abstract Theversatility of RNA seems limitless. The latest surprise comes from circularRNAs, which are found to counteract the function of another class of regulatoryRNA –the microRNAs.
摘要 RNA的多样性似乎没有边界。最新的惊奇来自环状RNA,发现它可以反作用于另一种调节性RNA-微RNA。
(正文)
信使RNA编码蛋白的功能可以被短的microRNA序列的结合而抑制。但microRNA诱导的抑制作用自身又是如何被抑制的一直不得而知。在本期中,Memczak等(333页)以及Hansen等(384页)描述了高度稳定的环状RNA通过结合几个拷贝的microRNA而终止microRNA抑制mRNA作用的过程。
报道的环状RNA(circRNA)有被Memczak称为CDR1as以及被Hanse称为ciRS-7的,包含可以与microRNA-7(miR-7)结合的大约70个结合位点的高度保守序列,并可以与AGO蛋白形成复合物。后一个环状RNA是RNA诱导沉默复合物的一部分,这个复合物使miRNA可以识别其目标mRNA。当Memczak与同事将人的CDR1as/ciRS-7表达在斑马鱼的胚胎中时,其效果与减少miR-7的表达时见到的一样-破坏了中脑的发育。还有,作者的生物信息预测指出在基因组中有几千个环状RNA的存在,这与之前的报道相一致。
miRNA所进行的目标抑制是一个有微妙之处的过程。一方面,miRNA上的这些序列可以诱导AGO-介导,通过mRNA与miRNA之间序列互补性激活的,在mRNA第10,11位核苷酸上的内切性核酸酶对mRNA的切割。在目标mRNA被切割后,miRNA被释放,重新以催化方式去与下一个目标结合。另一方面,miRNA可以通过化学计量的方式与目标mRNA结合得更紧密,这样miRNA就可以抑制蛋白的翻译。这种方式使目标mRNA变成了一个储存miRNA的“水库”,阻止miRNA进一步抑制其他mRNA。后一种机理说明了竞争性内源RNA(ceRNA)的作用方式。竞争性内源RNA(ceRNA)是一些mRNA,它们与其他mRNA一起分享miRNA-应答组份(MREs),因此与其它mRNA竞争性地与miRNA结合。
象内源性RNA一样,环状RNA也可以起miRNA水库的作用。然而由于环状RNA对于特异miRNA具有很多结合位点,因此其作用完全是为miRNA提供庇护所。内源性RNA与miRNA的结合不仅阻止了miRNA与其他MREs的结合,同时也可以抑制内援性RNA编码部分的翻译。这样,与环状RNA相比,内源性RNA以相对复杂的相互作用分子的方式限制翻译的进行。在特殊分子中也存在其他位点的水库。这些包括目标模拟物比如在植物拟南芥中的基因IPS1对于假基因PTENP1的诱饵作用,还有可能是与其相关蛋白编码序列分开的3’端mRNA未翻译区。
环状RNA通过消除RNA外切酶的活性来增加自身的稳定性,通常RNA外切酶在RNA分子自由3’或5’端开始进行切割。还有,由于一个环状RNA上有几个作为拮抗单一miRNA的结合位点,因此一个环状RNA就可以一下子从不同目标上抓到许多miRNA。同样,环状RNA的解体也可以一下子释放出很多miRNA,而这些miRNA会去寻找具有共同MRE的mRNA作为目标。事实上,Hansen等大致画出了环状RNA解体的机理,miR-671与互补性更强的CDR1as/ciRS-7结合而不是miR-7,导致AGO-介导对这一环状RNA的切割。
对miRNA进行快照法资料分析发现,miRNA的表达在发育,细胞分化或肿瘤形成的过渡点时期发生很大的变化。在这些过渡点阶段,可以通过环状RNA的方式清除mRNA-miRNA复合物而用另一种不同的miRNA代替。比如,作为一种蛮不讲理的方法来清除miRNA时,当细胞从干细胞开始进行分化时环状RNA增加表达,这样可以捕获在干细胞中过量表达的miRNA。环状RNA也可以清除成熟miRNA的另一条链,那条链可能以令人惊奇的数量存在;或者环状RNA可能具有治疗的功能,将癌症相关的miRNA从促进癌症形成的途径上移除。然而在所有这些情况中,环状RNA捕获miRNA,但miRNA是如何被解离得仍不得而知。
为了以最佳方式运转,每个环状RNA上大量的miRNA结合位点也许是在进化选择的压力下为了从其目标位点上进攻几乎所有某种特异的miRNA。如果情况真的如此,那么一个细胞中某种环状RNA上miRNA结合位点的数量与这种环状RNA的拷贝数的乘积将告诉我们某一个特异性miRNAMRE的总强调。许多miRNA在每个细胞中大约的拷贝数是103-大致上是将其完全清除所需环状RNA位点数的下界。然而,如果环状RNA要在与mRNA竞争miRNA的结合中取得胜利,它们就需要有比mRNA更强的与miRNA的亲和力。高亲和力可以通过热动力学的方式建立在环状RNA序列中,但还需要细胞中与其它相关性MREs总量相关的过量的环状RNA编码的miRNA的结合位点。确实,模型制作者将很快在这个领域中到处可见。
维护大致21个核苷酸长的miRNA没有改变在经过主要进化包括环形RNA后(图1)。对于每一个miRNA的选择压力无疑很高:一个miRNA的序列一定要自我成对形成发夹式miRNA前体;它一定要与目标mRNA配对;它也一定要与终结或调节目标相互结合的位点配对。虽然有大量的可能miRNA序列,miRNA数量上的改变很小,说明在剩余的进化空间中革新受到限制,换句话说,miRNA达到了分子的完美。在整个动物进化过程中,自然采用一套相对稳定的编码基因,而miRNA的革新,通常来讲,更离不开全新的序列的创造。也许发夹式miRNA前体轻而易举地以有效调节因素的方式出现-而且“数字式地”适合大量的基因组非编码序列,包括环状RNA-这种因素可能会成为进化的驱动者。
作为补充说明,我们需要一个更好的环状RNA的命名系统。“ciRS-7”说明它与miR-7结合,因此假设这类其他的环状RNA也会清除地对应一个miRNA。“CDR1as”假设这个环状RNA将与一个命名了的基因有某些联系-在这种情况下,是一个小脑变性相关基因的反义序列。基因组中有几千个这样的环状RNA,它们需要自己的编号系统,我建议把这个叫做circR-1。
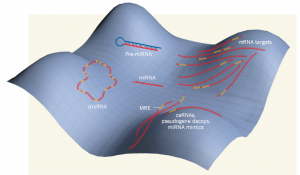
Figure 1 | Constraints on evolutionary change in microRNAs. MicroRNAs (miRNAs) liein a fitness valley constrained by their numerous interactions, which includethose with the hairpin structure of the precursor miRNA (pre-miRNA), the many targetmRNAs and other RNAs that terminate or modulate miRNA binding to targetsequences by competing against them. The latter category includes competingendogenous RNAs (ceRNAs), pseudogene decoys and miRNA mimics. Two studies1,2 introduce circular RNAs(circRNAs) as another constraining factor. MRE, miRNA-response element.
图1 microRNA 进化改变的限制。miRNA处于健身谷中,被大量的相互作用限制在那里,这些限制性的相互作用包括带有发夹结构的miRNA前体,许多目标mRNA和其他通过竞争来终结或调节miRNA与目标序列的结合的RNA。后面这类包括竞争性内源RNA(ceRNA),假基因诱饵以及miRNA模拟物。
(图中说明的是miRNA在进化过程中的各方面压力,因为评论的文章中侧重环状RNA对miRNA的作用,因此评论直接用miRNA的进化来说明。图本身很漂亮,属于比较fancy的那种。)
文章来源于“丁香园”





来第一个抢占沙发评论吧!