源于鼻咽上皮的鼻咽癌(NPC)在东南亚,北非,中东和阿拉斯加尤为普遍。由于NPC的隐匿症状和侵略性,超过70%的NPC患者而首次诊断即为局部晚期。根据NCCN指南,放疗联合化疗是局部晚期NPC(LA-NPC)的主要治疗策略,可显着减少局部复发性疾病。然而,远处转移仍然是NPC患者治疗失败的主要原因,并且是NPC患者死亡的主要原因。因此,进一步解决NPC转移的分子机制以开发更有效的治疗方案至关重要。越来越多的证据表明,全身诱导化疗(IC)可以有效消除NPC微转移并最终改善患者生存率。然而,患者对化疗的反应是不同的,有些患者会产生耐药性,导致治疗失败。该研究中,研究者使用RNA测序筛选到circCRIM1是在远处转移的NPC患者组织中显著上调的特定的circRNA。CircCRIM1通过充当miR-422a海绵来上调FOXQ1表达,从而促进NPC转移和多西他赛(Docetaxel、多烯紫杉醇)化学耐药性。此外,circCRIM1表达是一个独立的预后因素,当与N期结合使用时,可以区分具有远处转移和对基于多西他赛的全身化疗(IC)反应的NPC患者的不同风险。因此,这项研究表明,circCRIM1具有致癌作用,可能是预测NPC转移和化疗获益的有前途的标志物。
原文:Circular RNA CRIM1 functions as a ceRNA to promote nasopharyngeal carcinoma metastasis and docetaxel chemoresistance through upregulating FOXQ1 HONG ET AL. MOLECULAR CANCER (2020) http://sci-hub.tw/10.1186/s12943-020-01149-x
方案剖析
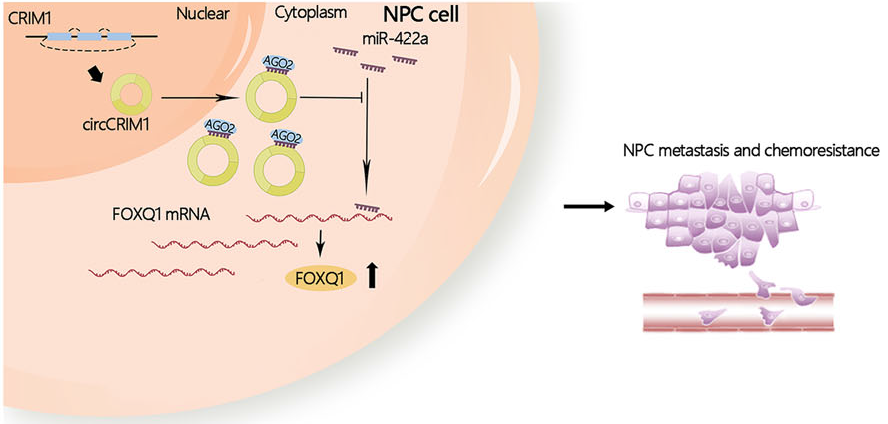
❀ 图:NPC中circCRIM1功能的假设模型
样本设计
人NPC细胞系(S18和S26),高转移性亚克隆S18和低转移性亚克隆S26
检测技术
芯片使用的是Affymetrix Human Genome U133 Plus 2.0 Array,数据来自于GSE12452(NP组织C),NPC细胞使用Agilent-046064 Unrestricted_Human_miRNA_V19.0_Microarray数据在GSE137312;使用Illumina HiSeqTM2000对NPC细胞系做了circular RNA-Sequencing (GSE137543)
数据分析
通过RNA测序分析发现了差异表达的circRNA,使用已发布的NPC数据集(GSE12452)进行了Gene set enrichment analysis (GSEA),使用P <0.05和FDR≤0.25的阈值选择显著结果。使用Receiver operating characteristic (ROC) 以确定用于circCRIM1高表达或低表达的分类的最佳临界值。使用Kaplan-Meier方法和对数秩检验构建生存曲线并比较差异。使用Cox比例风险回归模型,使用多变量分析确定独立的预后因素。
结论分享
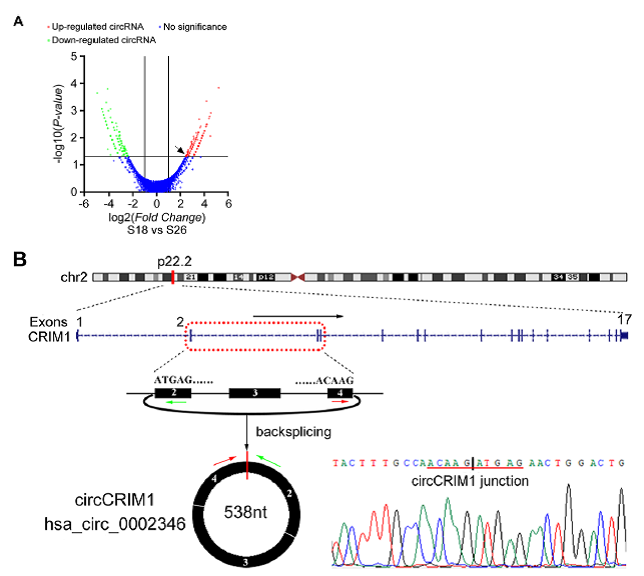
1) 最初针对人NPC细胞系(S18和S26)通过RNA 测序在高度转移的S18细胞系中找到了上调最明显的circRNA,即circCRIM1
2) 为了确定与circCRIM1相互作用的潜在miRNA,接下来进行了芯片分析,以评估S18和S26 NPC细胞的miRNA表达谱。结果显示高转移S18细胞系中有63个上调的miRNA和98个下调的miRNA(|倍数变化|≥3和FDR <0.05)。对下调的miRNA进行生物信息学算法miRanda,RNAhybrid和StarBase的预测,发现miR-422a和miR-4436a包含circCRIM1区域的假定靶向位点。然后,我们进行了荧光素酶检测,以验证这两个miRNA与circCRIM1的结合能力。
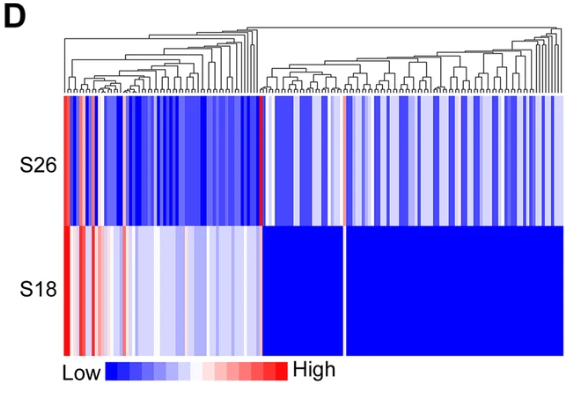
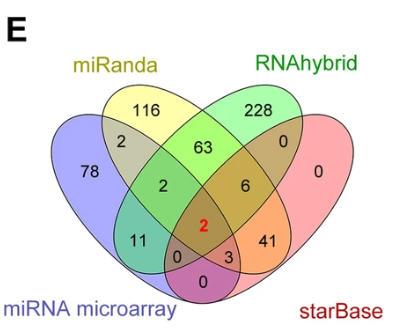
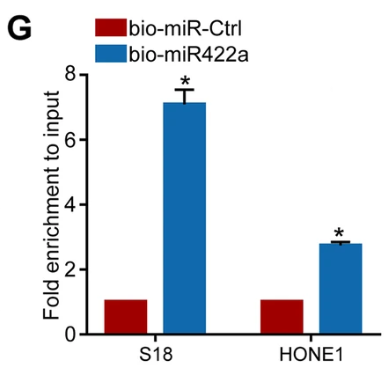
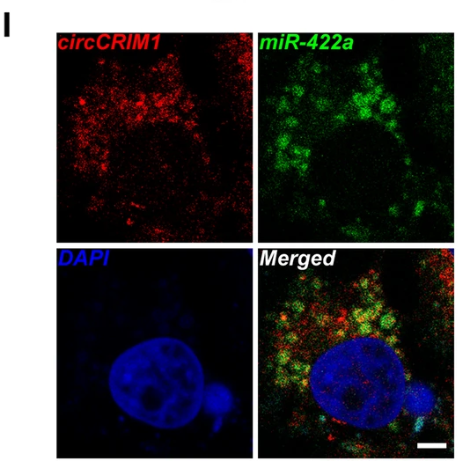
其它分析显示biotin-miR-422a显着提高了circCRIM1的富集度(P <0.05)。此外,双重FISH分析表明circCRIM1和miR-422a在NPC细胞中共定位。综上所诉,circCRIM1可以直接与miR-422a结合。
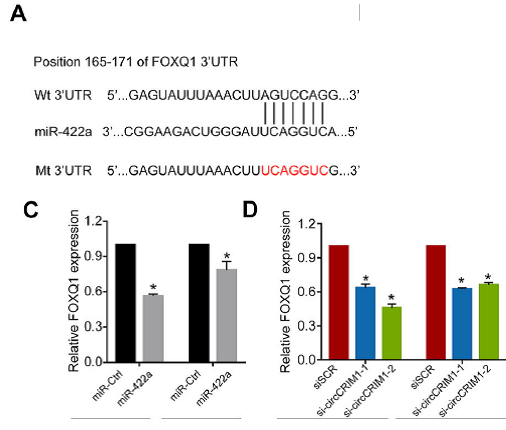
3) 最后采用了miRDB算法来探索circCRIM1和miR-422a的常见下游靶标,预计Forkhead box Q1 (FOXQ1) 是miR-422a的假定靶基因。qRT-PCR和蛋白质印迹分析表明,miR-422a过表达显着降低了FOXQ1 mRNA和蛋白水平。同样,circCRIM1耗竭显着抑制FOXQ1表达。相反,circCRIM1过表达显着增加了FOXQ1表达。这些数据表明FOXQ1可以由miR-422a和circCRIM1调节。
4)为了对具有远处转移风险的患者进行分层,作者基于circCRIM1表达状态和N期建立了预后预测模型。将患者分为3组:低风险组(低circCRIM1表达和早期N期)77例(35.3%),中风险组(高circCRIM1表达或晚期N期)92例(42.2%)高风险组(circCRIM1高表达和晚期N期)的患者(22.5%)。这三组患者的死亡,复发和远处转移的风险显着不同。此外,还评估了circCRIM1表达对于含多西他赛的IC敏感性表达状态和N期的预测值。这些发现表明,circCRIM1表达与N期的结合可能是一种有前途的特征,可以使用基于circCRIM1的预后模型来区分具有不同转移风险和对基于多西他赛的IC的治疗反应的患者。
总之,研究表明,circCRIM1通过海绵化miR-422a来发挥其ceRNA的功能,以调节下游FOXQ1的表达,从而促进了NPC的转移和基于多西他赛的IC化学耐药性(图6h)。




来第一个抢占沙发评论吧!